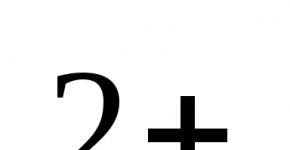Методика выполнения измерений биохимического потребления кислорода после -дней инкубации () в поверхностных пресных, подземных (грунтовых), питьевых, сточных и очищенных сточных водах. Манометрическое определение БПК Методика определения бпк5 в сточных во
В природной воде водоемов всегда присутствуют органические вещества. Их концентрации могут быть иногда очень малы (например, в родниковых и талых водах). Природными источниками органических веществ являются разрушающиеся останки организмов растительного и животного происхождения, как живших в воде, так и попавших в водоем с листвы, по воздуху, с берегов и т.п. Кроме природных, существуют также техногенные источники органических веществ: транспортные предприятия (нефтепродукты), целлюлозно-бумажные и лесоперерабатывающие комбинаты (лигнины), мясокомбинаты (белковые соединения), сельскохозяйственные и фекальные стоки и т.д. Органические загрязнения попадают в водоем разными путями, главным образом со сточными водами и дождевыми поверхностными смывами с почвы. В естественных условиях находящиеся в воде органические вещества разрушаются бактериями, претерпевая аэробное биохимическое окисление с образованием двуокиси углерода. При этом на окисление потребляется растворенный в воде кислород. В водоемах с большим содержанием органических веществ большая часть РК потребляется на биохимическое окисление, лишая таким образом кислорода другие организмы. При этом увеличивается количество организмов, более устойчивых к низкому содержанию РК, исчезают кислородолюбивые виды и появляются виды, терпимые к дефициту кислорода. Таким образом, в процессе биохимического окисления органических веществ в воде происходит уменьшение концентрации РК, и эта убыль косвенно является мерой содержания в воде органических веществ. Соответствующий показатель качества воды, характеризующий суммарное содержание в воде органических веществ, называется биохимическим потреблением кислорода (БПК).
Определение БПК основано на измерении концентрации РК в пробе воды непосредственно после отбора, а также после инкубации пробы. Инкубацию пробы проводят без доступа воздуха в кислородной склянке (т.е. в той же посуде, где определяется значение РК) в течение времени, необходимого для протекания реакции биохимического окисления. Так как скорость биохимической реакции зависит от температуры, инкубацию проводят в режиме постоянной температуры (20±1)°С, причем от точности поддержания значения температуры зависит точность выполнения анализа на БПК. Обычно определяют БПК за 5 суток инкубации (БПК 5), однако содержание некоторых соединений более информативно характеризуется величиной БПК за 10 суток или за период полного окисления (БПК 10 или БПК полн соответственно). Погрешность в определении БПК может внести также освещение пробы, влияющее на жизнедеятельность микроорганизмов и способное в некоторых случаях вызывать фотохимическое окисление. Поэтому инкубацию пробы проводят без доступа света (в темном месте).
Таблица. Величины БПК 5 в водоемах с различной степенью загрязненности
|
Степень загрязнения (классы водоемов) |
БПК 5 , мг 0 2 /дм 3 |
|
Очень чистые | |
|
Умеренно загрязненные | |
|
Загрязненные | |
|
Очень грязные |
Для водоемов, загрязненных преимущественно хозяйственно-бытовыми сточными водами, БПК 5 составляет обычно около 70% БПК П.
Определение БПКп в поверхностных водах используется с целью оценки содержания биохимически окисляемых органических веществ, условий обитания гидробионтов и в качестве интегрального показателя загрязненности воды. Необходимо использовать величины БПК5 при контроле эффективности работы очистных сооружений.
В зависимости от категории водоема величина БПК 5 регламентируется следующим образом: не более 3 мг О 2 /дм 3 для водоемов хозяйственно-питьевого водопользования и не более 6 мг О 2 /дм 3 для водоемов хозяйственно-бытового и культурного водопользования. Для морей (I и II категории рыбохозяйственного водопользования) пятисуточная потребность в кислороде (БПК 5) при 20°С не должна превышать 2 мг О 2 /дм 3 .
Полным биохимическим потреблением кислорода (БПК П) считается количество кислорода, требуемое для окисления органических примесей до начала процессов нитрификации. Количество кислорода, расходуемое для окисления аммонийного азота до нитритов и нитратов, при определении БПК не учитывается. Для бытовых сточных вод (без существенной примеси производственных) определяют БПК 20 , считая, что эта величина близка к БПК П.
Полная биологическая потребность в кислороде БПК П для внутренних водоемов рыбохозяйственного назначения (I и II категории) при 20°С не должна превышать 3 мг О 2 /дм 3 .
Пробоотбор и подготовка воды к анализу
Для проведения физико-химического анализа воды необходимо правильно провести пробоотбор. В зависимости от цели исследования проба воды для анализа может быть получена несколькими способами:
путем однократного отбора всего количества воды, нужного для анализа;
смешением проб, отобранных через определенные промежутки времени в одном месте исследуемого водоема;
смешением проб, отобранных одновременно в разных местах исследуемого водоема.
При отборе проб воды используют посуду из бесцветного стекла или полиэтилена марок, разрешенных для контакта с питьевой водой. Посуда должна быть тщательно вымыта моющими средствами, многократно ополоснута водопроводной и дистиллированной водой, а непосредственно перед забором воды посуду несколько раз ополаскивают исследуемой водой. Пробки желательно использовать стеклянные или полиэтиленовые; корковые или резиновые пробки обертывают полиэтиленовой пленкой.
На практике удобно пользоваться банкой или бутылью. В местах с затрудненным доступом к воде банку или бутыль можно прикрепить к шесту. Для взятия проб с определенной глубины используются батометры (рисунок). При отсутствии данного прибора можно сделать самодельный батометр, состоящий из бутыли (1л), с прикрепленным к ней тонким прочным шнуром необходимой длины. Бутыль закрывают пробкой со шнуром и помещают в футляр, имеющий груз и петлю. К петле привязывают веревку с отметками, указывающими глубину погружения. На нужной глубине выдергивают пробку из бутыли и после наполнения емкости водой и поднимают ее.
Отбор проб воды на проточных водоемах производится в 1 км выше ближайшего по течению пункта водопользования (водозабор для питьевого водоснабжения, места купания, организованного отдыха, территория населенного пункта), а на непроточных водоемах и водохранилищах - в 1 км в обе стороны от пункта водопользования.
Обычно пробы в створе отбирают в трех точках (у обоих берегов и в фарватере); при ограниченных же технических возможностях или на не-
больших водоемах допускается отбор проб в одной-двух точках (в местах наиболее сильного течения). Чаще всего пробы отбирают в 5 - 10 м от берега на глубине 50 см. Объектом особого внимания должны стать загрязненные струи.
Если на реке имеется сброс сточных вод от промышленных предприятий, стоки животноводческих ферм и т. д., то отбор проб воды проводят ниже сброса на 500 м, что позволяет контролировать степень загрязнения воды в реке сточными водами (для сравнения следует взять пробу на 500 м выше сброса сточных вод).
Если предполагается, что в результате сброса сточных вод в придонных слоях накапливаются оседающие вредные вещества, которые могут стать источником вторичного загрязнения воды, отбирают придонные пробы на расстоянии 30 - 50 см от дна.
В водохранилищах, озерах, прудах, где течение воды резко замедленно, качество воды может быть неоднородным на различных участках (здесь возможно возникновение вторичных источников загрязнения), поэтому в этих водоемах обычно берут серию проб по глубине.
Сразу же после взятия пробы необходимо сделать запись об условиях сбора, направлении ветра, указать дату и час отбора воды.
Подготовка воды к анализу
Для получения достоверных результатов анализ следует проводить возможно быстрее. В воде происходят процессы окисления-восстановления, физико-химические, биохимические, вызванные деятельностью микроорганизмов, сорбции, десорбции, седиментации и т. д. Могут изменяться и органолептические свойства воды - запах, цвет и др. Некоторые вещества способны адсорбироваться на стенках сосудов (железо, алюминий, медь, кадмий, марганец и др.), а из стекла бутылей могут выщелачиваться микроэлементы. При невозможности исследовать воду в установленные для соответствующих показателей сроки (таблица) ее охлаждают или консервируют.
Биохимические процессы в воде можно замедлить, охладив ее до 4°С. В этих условиях медленнее разрушаются и многие органические вещества.
Универсального консервирующего средства не существует, поэтому пробы для анализа отбирают в несколько бутылей. В каждой из них на месте отбора пробу консервируют, добавляя различные реагенты (таблица). Подготовка воды непосредственно перед анализом заключается в следующем:
Консервированные пробы при необходимости нейтрализуют, а охлажденные нагревают до комнатной температуры (не на нагревательном приборе);
Если определению мешают мутность и цветность, то проводят специальную подготовку: пробы фильтруют, отстаивают или коагулируют. Коагуляция проводится добавлением 5 мл суспензии гидроксида алюминия на 1 л воды, после чего смесь хорошо взбалтывают и дают отстояться.
Находящиеся в природной и питьевой воде загрязняющие вещества имеют, как правило, очень маленькие концентрации. Для того чтобы определить присутствие этих загрязнителей следует провести концентрирование этих примесей.
Если при анализе проводилось концентрирование пробы, то при последующих расчетах необходимо учитывать объем исходного образца воды.
Метод определения концентрации РК
Определение концентрации РК в воде проводится методом Винклера, который широко используется для санитарно-химического и экологического контроля.
3.2 Метод определения концентрации РК основан на способности гидроксида марганца (II) окисляться в щелочной среде до гидроксида марганца (IV), количественно связывая при этом кислород. В кислой среде гидроксид марганца (IV) снова переходит в двухвалентное состояние, окисляя при этом эквивалентное связанному кислороду количество йода. Выделившийся йод титруют раствором тиосульфата натрия в присутствии крахмала.
Определение РК проводится в несколько этапов. Сначала в анализируемую воду добавляют соль Мn (II), который в щелочной среде реагирует с растворенным кислородом с образованием нерастворимого гидроксида Мn (IV) по уравнению:
2Мn + О
+ О +4ОН
+4ОН = 2МnО(ОН)
= 2МnО(ОН)
 .
.
Таким образом, кислород «фиксируется» в пробе (количественно связывается). Кислород - неустойчивый компонент химического состава воды, поэтому фиксация должна быть проведена сразу после отбора пробы.
2МnО(ОН) + 6J
+ 6J +6Н
+6Н = Мn
= Мn + 3J
+ 3J + ЗН
+ ЗН О.
О.
Затем свободный йод титруют раствором тиосульфата натрия в присутствии крахмала, который добавляют в качестве индикатора для определения точки эквивалентности. Реакции описываются уравнениями:
J +2S
+2S O
O =2J
=2J +S
+S O
O
J + крахмал
+ крахмал
 синий краситель
.
синий краситель
.
В точке эквивалентности происходит обесцвечивание раствора.
3.3
По результатам титрования определяют
абсолютное содержание РК в воде в мг
О /л
и степень насыщения воды кислородом,
котораязависит
от температуры воды в момент отбора
пробы и атмосферного давления.
/л
и степень насыщения воды кислородом,
котораязависит
от температуры воды в момент отбора
пробы и атмосферного давления.
Метод определения биохимического потребления кислорода основан на способности микроорганизмов потреблять растворенный кислород при биохимическом окислении органических и неорганических веществ в воде.
Биохимическое
потребление кислорода определяют
количеством кислорода в мг/дм ,
которое требуется для окисления
находящихся вводе
углеродсодержащих органических веществ,
в аэробных условиях в
результате биохимических процессов.
,
которое требуется для окисления
находящихся вводе
углеродсодержащих органических веществ,
в аэробных условиях в
результате биохимических процессов.
3.5 По разности содержания РК в воде до и после инкубации пробы в кислородной склянке при стандартных условиях (продолжительность инкубации - 5 суток при температуре 20±1°С без доступа света и воздуха) определяют БПК. При этом пробу воды предварительноаэрируют для насыщения кислородом.
3.6
В поверхностных водах суши величина
БПКколеблется впределах
от 0,5 до 5 мг О /л,
она подвержена природным и суточнымизменениям,
которые в основном зависят от изменения
температуры и от
исходной концентрации растворенного
кислорода, связанные с физиологической
и биохимической активностью микроорганизмов.
Значительные
изменения БПК определяются степенью
загрязненности.
/л,
она подвержена природным и суточнымизменениям,
которые в основном зависят от изменения
температуры и от
исходной концентрации растворенного
кислорода, связанные с физиологической
и биохимической активностью микроорганизмов.
Значительные
изменения БПК определяются степенью
загрязненности.
3.7 Мешающее влияние на аналитическое определение РК могут оказывать вещества (взвешенные и окрашенные, биологически активные, восстановители, реагирующие с выделившимся йодом, окислители, выделяющие йод из йодида калия) в концентрациях, встречающихся только в сточных и загрязненных поверхностных водах.
3.8 Точность выполнения анализа определяется:
точностью отбора пробы;
качеством растворов, которое может ухудшиться при их загрязнении, хранении в негерметично закрытых склянках, в теплом месте или на свету, а также при хранении растворов слишком продолжительное время (без проведения периодического контроля);
чистотой используемой посуды для отбора проб и выполнения нализов;
полнотой учета мешающих примесей, которые могут присутствовать в анализируемой воде;
ошибками при титровании.
Меры безопасности
При работе с комплектом в полевых и лабораторных условиях руководствуются основными правилами техники безопасности, предусмотренными для химико-аналитических работ.
4.2 Методика выполнения анализа предусматривает использование щелочного раствора йодида калия и раствора серной кислоты. Следует избегать попадания щелочного и сернокислотного растворов на слизистые оболочки, кожные покровы, одежду, обувь, оборудование и т.п. При попадании на кожу или слизистые оболочки следует быстро и обильно промыть водой, при необходимости обратиться к специалисту в медицинское учреждение.
4.3. Едкие вещества требуют особого обращения:
хранения в специальном месте, недоступном для неспециалистов:
использования их только оператором (преподавателем);
учета при расходовании.
Подготовка к проведению анализа
Подготовка к проведению анализа включает: проверку целостности мерной и др. посуды; проверку наличия растворов в склянках; приготовление растворов.
Раствор крахмала неустойчив при хранении. Для приготовления свежего - растворите содержимое капсулы в 10-15 мл холодной дистиллированной воды, полученную суспензию постепенно прилейте к 35-40 мл кипящей дистиллированной воды и кипятите 2-3 минуты. Раствор охладите.
По мере использования рабочего раствора тиосульфата натрия (0,02 моль/л экв.) приготовьте новый. Отберите мерной пипеткой 20,0 мл раствора тиосульфата натрия (0,1 моль/л экв.), поместите в мерную колбу вместимостью 100 мл, доведите объем раствора до метки дистиллированной водой, перемешайте раствор.
Оборудование и реактивы: Барометр любого типа; груша резиновая или медицинский шприц; колба коническая вместимостью 250–300 мл; склянка кислородная калиброванная (100–200 мл) с пробкой; мешалка (стеклянные шарик, палочка и т.п.) известного объема; пипетки мерные на 1 мл и 10 мл; термометр; раствор соли марганца; раствор серной кислоты (1:2); раствор тиосульфата натрия (0,02 моль/л экв.); раствор крахмала (0,5%); раствор йодида калия щелочной.
Проведение анализа
1. Добавьте в склянку с пробой анализируемой воды разными пипетками 1 мл раствора соли марганца, 1 мл раствора йодида калия, погружая пипетку с раствором в кислородную склянку на глубину 2-3 см, как показано на рисунке и по мере выливания раствора поднимайте пипетку вверх.

Излишек жидкости из склянки стечет через край на подставленную чашку Петри.

Слегка наклоните склянку, закройте пробкой. Излишек жидкости стечет через край. Следите, чтобы в склянке не осталось пузырьков воздуха.
Склянка не должна оставаться открытой.

2. Перемешайте содержимое склянки имеющейся внутри мешалкой, удерживая склянку рукой. Поместите склянку с зафиксированной пробой в темное место для отстаивания (не менее 10 минут и не более 24 часов).

Добавьте пипеткой 2 мл раствора серной кислоты.
Закройте склянку пробкой и перемешайте содержимое до полного растворения осадка.

5. Перенесите содержимое склянки в коническую колбу для титрования вместимостью 250 мл.
Примечание. Можно проводить титрование части пробы. Для этого из кислородной склянки в колбу для титрования перенесите цилиндром 50,0 мл обработанной пробы.

6. Заполните пипетку (бюретку), закрепленную в стойке-штативе раствором тиосульфата натрия (0,02 моль/л экв.) и титруйте пробу до слабо желтой окраски. Затем добавьте пипеткой 1 мл раствора крахмала (раствор в колбе синеет) и продолжайте титровать до полного обесцвечивания раствора.

7. Определите общий объем раствора тиосульфата натрия, израсходованного на титрование (как до, так и после добавления раствора крахмала).

БИОХИМИЧЕСКОЕ ПОТРЕБЛЕНИЕ КИСЛОРОДА В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ СКЛЯНОЧНЫМ
МЕТОДОМ
Ростов-на-Дону
2006
Предисловие
1. РАЗРАБОТАН ГУ «Гидрохимический институт»
2. РАЗРАБОТЧИКИ А.А. Назарова, канд. хим. наук, Ю.А. Андреев
3. СОГЛАСОВАН с Начальником УМЗА и ГУ «ЦКБ ГМП» Росгидромета
5. АТТЕСТОВАН ГУ «Гидрохимический институт», свидетельство об аттестации № 73.24-2005 от 15.06.2005 г.
6. ЗАРЕГИСТРИРОВАН ГУ ЦКБ ГМП за номером РД 52.24.420-2006 от 30.03.2006 г.
Внесен в Федеральный реестр методик выполнения измерений, применяемых в сферах распространения государственного метрологического контроля и надзора за номером ФР. 1.31.2006.02517
7. ВЗАМЕН РД 52.24.420-95 «Методические указания. Методика выполнения измерений биохимического потребления кислорода в водах скляночным методом».
Введение
Находящиеся в воде микроорганизмы в процессе своей жизнедеятельности используют растворенный в воде кислород для биохимического окисления органических соединений, в том числе загрязняющих веществ. Количество кислорода, израсходованное в определенный промежуток времени в процессе биохимического окисления органических веществ, содержащихся в анализируемой воде, называется биохимическим потреблением кислорода (далее - БПК). Этот показатель является некоторой условной мерой загрязнения вод органическими соединениями, в особенности достаточно легко подвергающимися биохимической деградации.
Скорость биодеградации органических загрязняющих веществ зависит от множества факторов. В среднем можно полагать, что при 20 °C за 5 сут. окисляется около 70 % соединений, за 10 и 20 сут. - соответственно 90 % и 99 %. Однако для практических целей полное окисление слишком длительно и его как правило не используют. При неполном окислении органических веществ для сопоставимости величин БПК его определение должно проводиться в некоторых стандартных условиях. В качестве таковых приняты следующие: продолжительность инкубации 5 сут., температура (20 ± 1) °C, отсутствие доступа света и воздуха. Потребление кислорода, определенное при этих условиях называется пятисуточным биохимическим потреблением кислорода (БПК 5). Его находят как разность между содержанием кислорода в анализируемой пробе воды до и после инкубации.
При определении БПК 5 необходимо также соблюдать условия, при которых количество кислорода в пробе в течение инкубации соответствовало бы его потреблению. Это зависит от таких факторов, как степень разбавления проб с большим биохимическим потреблением кислорода, применение одной и той же разбавляющей воды и способ обработки пробы воды. Содержание кислорода в анализируемой исходной или разбавленной пробе должно оставаться в течение всего времени инкубации таким, чтобы были обеспечены хорошие условия для протекания аэробных биохимических процессов. Это будет соблюдено, если анализируемая проба или смесь пробы с разбавляющей водой перед определением будут содержать равновесную с воздухом концентрацию кислорода (около 9 мг/дм 3 при 20 °C), если минимальное потребление кислорода будет не менее 2 мг/дм 3 , а оставшаяся спустя 5 сут. концентрация кислорода - не менее 3 мг/дм 3 .
Величина БПК 5 для водных объектов рыбохозяйственного назначения нормируется (не более 2 мг/дм 3 О 2).
РУКОВОДЯЩИЙ ДОКУМЕНТ
|
БИОХИМИЧЕСКОЕ ПОТРЕБЛЕНИЕ КИСЛОРОДА В ВОДАХ. МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ СКЛЯНОЧНЫМ МЕТОДОМ |
Дата введения 2006-04-01
1. Область применения
1.1. Настоящий руководящий документ устанавливает методику выполнения измерений (далее - методика) БПК 5 в пробах поверхностных вод суши и очищенных сточных вод скляночным методом при содержании органических веществ, эквивалентном потреблению кислорода в диапазоне от 1,0 до 11,0 мг/дм 3 . При значении БПК 5 более 6,0 мг/дм 3 определение следует проводить при соответствующем разбавлении пробы.
1.2. Настоящий руководящий документ предназначен для использования в лабораториях, осуществляющих анализ поверхностных вод суши и очищенных сточных вод.
2. Нормативные ссылки
В настоящем руководящем документе использованы ссылки на следующие нормативные документы:
3. Приписанные характеристики погрешности измерений
3.1. При соблюдении всех регламентируемых методикой условий проведения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице .
Таблица 1 - Диапазон измерений, значения характеристик погрешности и ее составляющих
4.1.4. Пипетки градуированные 2 класса точности исполнения 1, 2 по ГОСТ 29227-91 вместимостью:
|
1 см 3 - 5 шт. |
|
|
2 см 3 - 2 шт. |
|
|
5 см 3 - 1 шт. |
4.1.5. Пипетка с одной отметкой 2 класса точности исполнения 1, 2 по ГОСТ 29169-91 вместимостью:
4.1.7. Цилиндры мерные, исполнения 1, 3 по ГОСТ 1770-74 вместимостью:
|
10 см 3 - 1 шт. |
|
|
50 см 3 - 1 шт. |
|
|
100 см 3 - 1 шт. |
|
|
250 см 3 - 1 шт. |
|
|
500 см 3 - 1 шт. |
|
|
1000 см 3 - 1 шт. |
4.1.8. Колбы конические исполнения 1, 2 по ГОСТ 25336-82 вместимостью:
4.1.10. Стаканы химические, тип В, исполнения 1, ТХС по ГОСТ 25336-82 вместимостью:
|
50 см 3 - 1 шт. |
|
|
100 см 3 - 1 шт. |
|
|
250 см 3 - 1 шт. |
|
|
600 см 3 - 1 шт. |
|
|
1000 см 3 - 1 шт. |
4.1.11. Склянки с притертыми пробками (кислородные) для проб воды вместимостью 100 - 250 см 3 (или склянки БПК).
4.1.12. Элемент ЭП1 (трубка хлоркальциевая) по ГОСТ 25336-82 - 1 шт.
4.1.13. Стаканчики для взвешивания (бюксы) СВ-19/9 по ГОСТ 25336-82 - 2 шт.
4.1.14. Воронка лабораторная по ГОСТ 25336-82 диаметром 75 мм - 1 шт.
4.1.15. Колба с тубусом (Бунзена) исполнения 1, 2 по ГОСТ 25336-82 вместимостью 0,25 - 0,5 дм 3 - 1 шт.
4.1.16. Воронка Бюхнера 1 или 2 по ГОСТ 9147-80
4.1.17. Термостат для проб, поддерживающий температуру (20 ± 1) °C.
4.1.18. Насос вакуумный любого типа.
4.1.19. Палочка стеклянная
4.1.20. Флаконы с пробками стеклянные для хранения реактивов вместимостью 100 см 3 , 100 см 3 , 500 см 3 .
4.1.21. Посуда стеклянная и полиэтиленовая для хранения проб и реактивов вместимостью 0,1; 0,25 и 1 дм 3 .
4.1.22. Шпатель (стеклянная лопатка).
4.1.23. Кюветы фотографические или кристаллизатор.
4.1.24. Отрезок гибкой пластиковой трубки длиной 50 - 70 см (сифон).
4.1.25. Микрокомпрессор аквариумный.
4.1.26. Холодильник бытовой.
4.1.27. Шкаф сушильный общелабораторного назначения.
4.1.28. Электроплитка по ГОСТ 14919-83 .
Допускается использование других типов средств измерений, вспомогательных устройств, в том числе импортных, с характеристиками не хуже, чем у приведенных в .
4.2. Реактивы и материалы
При выполнении измерений применяют следующие реактивы и материалы:
4.2.1. Марганец (II) хлористый 4-водный (хлорид марганца) по ГОСТ 612-75 , ч.д.а. или марганец (II) сернокислый 5-водный (сульфат марганца) по ГОСТ 435-77 , ч.д.а. (допустимо ч.).
4.2.2. Калий йодистый (йодид калия) по ГОСТ 4232-74 , ч.д.а. или натрий йодистый 2-водный (йодид натрия) по ГОСТ 8422-76 , ч.д.а.
4.2.18. Вода дистиллированная по ГОСТ 6709-72 , свежепрокипяченная и охлажденная в закрытой склянке до комнатной температуры.
4.2.19. Универсальная индикаторная бумага по ТУ 6-09-1181-77.
4.2.20. Фильтры обеззоленные «белая лента» и «синяя лента» по ТУ 6-09-1678-86.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в .
5. Метод измерений
Определение основано на измерении массовой концентрации растворенного кислорода скляночным методом путем йодометрического титрования в первоначальной или разбавленной пробе воды до и после ее инкубации в течение 5 сут. при стандартных условиях (20 °C, отсутствие доступа воздуха и света).
6. Требования безопасности, охраны окружающей среды
6.1. При выполнении измерений БПК 5 в пробах поверхностных вод суши и очищенных сточных вод соблюдают требования безопасности, установленные в национальных стандартах и соответствующих нормативных документах.
6.2. По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2, 3 классам опасности по ГОСТ 12.1.007 .
6.3. Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005 .
6.4. Дополнительных требований по экологической безопасности не предъявляется.
7. Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица со средним профессиональным образованием или без профессионального образования, но имеющие стаж работы в лаборатории не менее года и освоившие методику.
8. Условия выполнения измерений
8.1. При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
Температура окружающего воздуха (22 ± 5) °C;
Атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт. ст.);
Влажность воздуха не более 80 % при 25 °C;
Напряжение в сети (220 ± 10) В;
Частота переменного тока в сети питания (50 ± 1) Гц.
9. Отбор и хранение проб
Отбор проб производится в соответствии с ГОСТ 17.1.5.05 и ГОСТ Р 51592 . Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ Р 51592 .
Определяемое значение БПК 5 в значительной степени зависит от особенностей химических и биохимических процессов, протекающих в пробе в промежутке времени между ее отбором и началом анализа. Пробы для определения БПК 5 консервировать не допускается. Поэтому пробу необходимо обрабатывать сразу же после отбора, как описано в разделе . Если это невозможно, то отбирают пробу воды в посуду темного стекла, заполняя склянку под горло и хранят при температуре не выше 4 °C не более 4 ч.
10. Подготовка к выполнению измерений
10.1. Приготовление растворов и реактивов
10.1.1. Раствор хлорида (сульфата) марганца
Растворяют 210 г хлорида марганца (М n Сl 2 · 4Н 2 О) или 260 г сульфата марганца (MnSO 4 · 5H 2 O) или 290 г сульфата марганца (MnSO 4 · 7H 2 O) в 300 - 350 см 3 дистиллированной воды, фильтруют в мерную колбу вместимостью 500 см 3 и доливают дистиллированной водой до метки на колбе. Хранят в плотно закрытой склянке.
10.1.2. Щелочной раствор йодида калия (или натрия)
Растворяют 15 г йодида калия или 18 г йодида натрия (NaI · H 2 O) в 20 см 3 , а 50 г гидроксида натрия - в 50 см 3 дистиллированной воды.
Полученные растворы смешивают в мерной колбе вместимостью 100 см 3 и доводят объем дистиллированной водой до метки на колбе. При наличии мути раствор фильтруют. Хранят в склянке из темного стекла с плотной резиновой пробкой.
10.1.3. Раствор соляной кислоты 2:1 (по объему)
К 170 см 3 дистиллированной воды 340 см 3 концентрированной соляной кислоты добавляют.
Вместо раствора соляной кислоты 2:1 (по объему) во всех случаях можно использовать раствор серной кислоты 1:4 (по объему). Для его приготовления 100 см 3 концентрированной серной кислоты добавляют к 400 см 3 дистиллированной воды.
ВНИМАНИЕ! СЕРНУЮ КИСЛОТУ ОТМЕРИВАЮТ СУХИМ ЦИЛИНДРОМ И ОСТОРОЖНО ПРИЛИВАЮТ К ДИСТИЛЛИРОВАННОЙ ВОДЕ НЕБОЛЬШИМИ ПОРЦИЯМИ ПРИ ПЕРЕМЕШИВАНИИ (В ТЕРМОСТОЙКОМ СТАКАНЕ).
Проверку чистоты растворов хлорида марганца, йодида калия (или натрия), соляной (или серной) кислоты и их очистку осуществляют, как описано в .
10.1.4. Раствор крахмала, 0,5 %-ный
Взбалтывают 0,5 г крахмала с 15 - 20 см 3 дистиллированной воды.
Суспензию постепенно приливают к 80 - 85 см кипящей дистиллированной воды и кипятят еще 2 - 3 мин. После охлаждения раствора его консервируют добавлением 2 - 3 капель хлороформа или нескольких кристалликов салициловой кислоты.
Раствор используют до помутнения.
10.1.5. Раствор дихромата калия с молярной концентрацией количества вещества эквивалента (КВЭ) 0,0200 моль/дм 3
При использовании стандарт-титра (см. ) последний переносят в мерную колбу вместимостью 500 см 3 , растворяют в дистиллированной воде и доводят до метки. Затем пипеткой с одной отметкой отбирают 50 см 3 полученного раствора, переносят его в мерную колбу вместимостью 500 см 3 и доводят объем дистиллированной водой до метки.
При отсутствии стандарт-титра для приготовления стандартного раствора взвешивают 0,4904 г дихромата калия, предварительно высушенного в сушильном шкафу при температуре 105 °C в течение 1 - 2 ч, количественно переносят в мерную колбу вместимостью 500 см 3 , растворяют в дистиллированной воде и доводят объем раствора до метки на колбе. Хранят в склянке с притертой пробкой в темном месте не более 6 мес.
10.1.6. Раствор тиосульфата натрия с молярной концентрацией КВЭ 0,02 моль/дм 3
При использовании стандарт-титра (см. ) последний переносят в мерную колбу вместимостью 500 см 3 , растворяют в дистиллированной воде и доводят до метки. Затем пипеткой с одной отметкой отбирают 50 см 3 полученного раствора, переносят его в мерную колбу вместимостью 500 см 3 и доводят объем дистиллированной водой до метки.
Для приготовления стандартного раствора из навески при отсутствии стандарт-титра 2,5 г тиосульфата натрия (Na 2 S 2 O 3 · 5H 2 O) переносят в мерную колбу вместимостью 500 см 3 , растворяют в дистиллированной воде и доводят объем раствора до метки на колбе.
В качестве консерванта к полученному раствору добавляют 3 см 3 хлороформа. Перед определением точной концентрации раствор выдерживают не менее 5 сут. Хранят в склянке из темного стекла, закрытой пробкой с вставленными в нее сифоном с бюреткой и хлоркальциевой трубкой, заполненной гранулированным гидроксидом калия или гидроксидом натрия.
Точную концентрацию стандартного раствора тиосульфата натрия определяют, как описано в не реже 1 раза в неделю. Результаты проверки заносят в специальный журнал.
В 500 см 3 дистиллированной воды растворяют 0,13 г хлорида железа (FeCl 3 · 6H 2 O).
Разбавляющую воду готовят в день применения из дистиллированной воды с температурой 20 °C, добавляя фосфатный буферный раствор, растворы сульфата магния, хлорида кальция и хлорида железа (см. - ) из расчета по 1 см 3 на 1 дм 3 .
Затем насыщают воду кислородом воздуха интенсивным встряхиванием, после чего оставляют на 3 - 5 мин (до исчезновения мелких пузырьков воздуха) для установления равновесия.
Все растворы, необходимые для приготовления разбавляющей воды, хранят до появления в них осадка или до повышения значения БПК разбавляющей воды более 0,5 мг/дм 3 (см. ).
10.1.12. Раствор соляной кислоты, 1 моль/дм 3
К 92 см 3 дистиллированной воды добавляют 8,5 см 3 концентрированной соляной кислоты и перемешивают.
10.1.13. Раствор гидроксида натрия, 1 моль/дм 3
В 100 см 3 дистиллированной воды растворяют 4 г гидроксида натрия. Хранят в полиэтиленовой посуде.
10.2. Проверка чистоты и очистка используемых реактивов и растворов
10.2.1. Йодид калия (натрия)
Для проверки чистоты 1 г йодида калия растворяют в 100 см 3 свежепрокипяченной и охлажденной до комнатной температуры дистиллированной воды, приливают 10 см 3 раствора соляной кислоты, проверенной на чистоту, и 1 см 3 раствора крахмала.
Если в течение 5 мин голубая окраска не появляется, реактив пригоден для использования. В противном случае йодид калия должен быть очищен от свободного йода.
Для этого 30 - 40 г йодида калия помещают в воронку Бюхнера и промывают при перемешивании охлажденным до 3 - 5 °C этиловым спиртом до появления бесцветной порции последнего. Промытый йодид калия сушат в темноте между листами фильтровальной бумаги в течение суток. Хранят в плотно закрытой склянке из темного стекла.
Проверку чистоты и очистку йодида натрия проводят аналогичным образом.
10.2.2. Раствор хлорида (сульфата) марганца
К 100 см 3 свежепрокипяченной и охлажденной дистиллированной воды добавляют 1 см 3 раствора соли марганца, 0,2 г сухого йодида калия, 5 см 3 раствора соляной кислоты, проверенных на чистоту, и 1 см 3 раствора крахмала.
Отсутствие через 10 мин синей окраски указывает на чистоту реактива. В противном случае для очистки раствора на каждые 100 см 3 его добавляют около 1 г безводного карбоната натрия, хорошо перемешивают, отстаивают в течение суток, а затем фильтруют через бумажный фильтр «синяя лента».
10.2.3. Раствор кислоты (соляной или серной)
К 50 см 3 дистиллированной воды добавляют 1 см 3 раствора крахмала, 1 г проверенного на чистоту йодида калия и 10 см 3 раствора соляной кислоты.
Если в течение 5 мин не появится синяя окраска, кислота может быть использована в анализе, в противном случае следует заменить исходный реактив.
10.3. Установление точной вместимости кислородных склянок
Чтобы установить вместимость склянки для определения кислорода, ее тщательно моют, высушивают (снаружи и изнутри) и взвешивают вместе с пробкой с точностью до 0,01 г. Предварительно склянки выдерживают в комнате для взвешивания не менее 30 мин.
Затем наполняют ее дистиллированной водой до краев и закрывают стеклянной пробкой так, чтобы под пробкой не оставалось пузырьков воздуха. Обтирают склянку досуха и снова взвешивают с точностью до 0,01 г. Дистиллированную воду также выдерживают в комнате для взвешивания не менее 30 мин и измеряют ее температуру.
По разности двух взвешиваний рассчитывают массу воды в склянке, которую для перевода в объем следует разделить на коэффициент, равный 0,998 при температуре воды 15 °C, 0,997 - при 20 °C и 0,996 - при 25 °C.
10.4. Определение точной концентрации раствора тиосульфата натрия
В колбу для титрования вносят 80 - 90 см 3 дистиллированной воды, 10 см 3 раствора дихромата калия, 0,0200 моль/дм 3 КВЭ, добавляют 1 г сухого йодида калия и 10 см 3 раствора соляной кислоты. Раствор перемешивают, выдерживают 5 мин в темном месте и титруют раствором тиосульфата натрия до светло-желтой окраски. Затем добавляют 1 см 3 раствора крахмала и продолжают титрование до исчезновения синей окраски. Повторяют титрование и, если расхождение между значениями объемов титранта не более 0,05 см 3 , за результат принимают их среднее.
В противном случае повторяют титрование до получения результатов, отличающихся не более, чем на 0,05 см 3 .
Точную молярную концентрацию КВЭ тиосульфата натрия в растворе рассчитывают по формуле
(2)
где C m - молярная концентрация раствора тиосульфата натрия, моль/дм 3 КВЭ;
C д - молярная концентрация раствора дихромата калия, моль/дм 3 КВЭ;
V т
V д - объем раствора дихромата калия, взятый для титрования, см 3 .
11. Выполнение измерений
11.1. Заполнение и инкубация склянок
Если проба не содержит визуально заметного количества взвешенных веществ, 1,0 - 1,4 дм 3 ее помещают в достаточно большую (2 дм 3) колбу, устанавливают pH в пределах 6 - 8 по универсальной индикаторной бумаге добавлением раствора соляной кислоты или гидроксида натрия 1 моль/дм 3 . Доводят температуру пробы до (20 ± 1) °C, нагревая (при помощи водяной бани) или охлаждая ее (под струей водопроводной воды). Затем энергично взбалтывают пробу не менее 10 мин, чтобы насытить ее кислородом. Насыщение пробы кислородом можно также осуществить, пропуская через нее воздух с помощью аквариумного микрокомпрессора. После завершения процедуры насыщения пробу следует оставить на 3 - 5 мин для удаления избытка воздуха (до отсутствия поднимающихся к поверхности мелких пузырьков).
Если проба содержит грубую взвесь, ее наливают в склянку (лучше, цилиндр) вместимостью не менее 1 дм 3 и отстаивают 0,5 - 1 ч. После отстаивания отбирают сифоном осветлившийся средний слой воды в колбу для насыщения кислородом. Если пробу отстаиванием в течение часа осветлить не удается, ее фильтруют через бумажный фильтр «белая лента». Всегда в результатах анализа следует указывать принятый способ предварительной обработки воды.
Подготовленную пробу наливают в 3 сухие кислородные склянки, заполняя их до края так, чтобы внутри склянки не образовывалось пузырьков. В одной из 3-х склянок сразу же фиксируют и определяют концентрацию растворенного кислорода (см. ). Время между аэрацией пробы и фиксированием кислорода при определении его концентрации не должно быть более 15 мин.
Две другие склянки закрывают, помещают пробками вниз в наполненную дистиллированной водой фотографическую кювету или кристаллизатор (гидрозатвор) и устанавливают в термостат. При использовании склянок БПК колпачок заполняется той же пробой. Склянки выдерживают при отсутствии доступа света в термостате при (20 ± 1) °C в течение 5 сут. По истечении этого срока в инкубированных склянках определяют концентрацию неизрасходованного растворенного кислорода (см. ).
11.2. Определение растворенного кислорода
Сразу же после заполнения склянки (или после инкубации) фиксируют растворенный кислород, для чего в склянку с пробой воды вводят отдельными пипетками 1 см 3 (при вместимости склянки до 150 см 3) или 2 см 3 (при вместимости более 150 см 3) растворахлорида (сульфата) марганца и 1 см 3 или 2 см 3 щелочного раствора йодида калия (при вместимости склянки до 150 см 3 и более 150 см 3 соответственно).
Пипетку погружают каждый раз до половины склянки и поднимают вверх по мере истечения реактива из нее. Затем быстро закрывают склянку стеклянной пробкой таким образом, чтобы в ней не оставалось пузырьков воздуха, и содержимое тщательно перемешивают 15 - 20-кратным переворачиванием склянки до равномерного распределения осадка в воде по всему объему склянки. Склянки с зафиксированным в них кислородом помещают в темное место для отстаивания (на время не менее 10 мин и не более 24 ч).
После того, как опустившийся на дно осадок будет занимать менее половины высоты склянки, к пробе приливают 5 или 10 см 3 (в зависимости от вместимости склянки) раствора соляной кислоты, погружая при этом пипетку до дна склянки к осадку (не взмучивать) и медленно поднимая ее вверх по мере опорожнения. Вытеснение из склянки части прозрачной жидкости для анализа значения не имеет.
Склянку закрывают пробкой, и содержимое тщательно перемешивают. После полного растворения бурого осадка пипеткой с одной отметкой отбирают 50 см 3 раствора, предварительно ополаскивая пипетку этим же раствором, переносят его в колбу для титрования и титруют раствором тиосульфата натрия из бюретки вместимостью 10 см 3 до тех пор, пока он не станет светло-желтым. Затем прибавляют 1 см 3 раствора крахмала и продолжают титрование до исчезновения синей окраски.
В склянках после инкубации, повторяют определение растворенного кислорода, отбирая аликвоту из второй (следующей) склянки.
11.3. Разбавление проб
Если предполагается, что значение БПК 5 будет больше 5 мг/дм 3 , то растворенного кислорода может не хватить для окисления органического вещества пробы. В этом случае исходную пробу разбавляют. Для разбавления используют воду, подготовленную в соответствии с .
В зависимости от предполагаемого значения БПК 5 при разбавлении для выбора объема пробы анализируемой воды руководствуются таблицей .
|
Объем пробы воды в 1 дм 3 смеси, см 3 |
Степень разбавления |
|
Для ориентировочной оценки степени разбавления пробы можно использовать значение перманганатной окисляемости, бихроматной окисляемости (ХПК), органолептические (характер и интенсивность запаха пробы) или визуальные показатели (наличие, а также возможный состав взвешенного вещества).
Если значение БПК 5 совершенно неизвестно, следует делать несколько последовательных разбавлений, например 1:1, 1:4, 1:9, то есть в 2, 5, 10 раз, соответственно.
Разбавление пробы следует проводить в мерной колбе вместимостью 1000 см 3 и доливать до метки разбавляющей водой. Точный объем пробы отмеривают пипеткой (до 50 см 3) или цилиндром (более 50 см 3).
Затем поступают в соответствии с
Подготовленные при разбавлении пробы должны иметь температуру (20 ± 1) °C и значение pH 6 - 8.
Если при определении БПК 5 проводили разбавление проб, следует одновременно заполнить 4 кислородные склянки водой для разбавления проб (см. ). В двух из них сразу же определяют концентрацию растворенного кислорода, а две другие помещают в термостат вместе с партией анализируемых проб и определяют в них концентрацию растворенного кислорода после инкубации. Разница средней концентрации кислорода в исходных и инкубированных пробах разбавляющей воды не должна превышать 0,5 мг/дм 3 .
Полученную поправку учитывают при расчете значения БПК 5 (см. ). При более высоком значении БПК 5 разбавляющей воды результаты определения будут недостоверны, и следует заменить воду для разбавления более чистой, повторить отбор проб и определение БПК 5 .
11.4. Подготовка проб при наличии в воде активного хлора
К пробам, подвергавшимся обработке хлором или хлорной известью и содержащим активный хлор, перед началом определения БПК 5 добавляют необходимый для его полного восстановления объем раствора тиосульфата натрия, который определяют следующим образом.
В колбу для титрования вносят 100 см 3 анализируемой воды, 1 г сухого йодида калия, 10 см 3 раствора соляной кислоты, тщательно перемешивают и титруют раствором тиосульфата натрия до светло-желтого цвета, а затем после добавления 1 см 3 раствора крахмала - до полного обесцвечивания.
12. Вычисление и оформление результатов измерений
12.1. Массовую концентрацию растворенного в воде кислорода X , мг/дм 3 , находят по формуле
![]() (3)
(3)
где М - молярная масса КВЭ кислорода, равная 8 мг/ммоль.
C т - концентрация раствора тиосульфата натрия, моль/дм 3 КВЭ;
V т - объем раствора тиосульфата натрия, пошедший на титрование, см 3 ;
V - вместимость кислородной склянки, см 3 .
V 1 - суммарный объем растворов хлорида марганца и йодида калия, добавленных в склянку при фиксации растворенного кислорода, см 3 ;
БПК 5 = Х и - Х к
или
![]() (4)
(4)
где Х н - массовая концентрация растворенного кислорода в пробе анализируемой воды (или разбавляющей воды) до инкубации, мг/дм 3 ;
Х к - массовая концентрация растворенного кислорода в пробе анализируемой воды (или разбавляющей воды) после 5 сут. инкубации, мг/дм 3 ;
12.3. Биохимическое потребление кислорода БПК 5 , мг/дм 3 , для подвергавшихся разбавлению проб находят по формуле
(5)
где Х н - концентрация растворенного кислорода в пробе анализируемой воды до инкубации, мг/дм 3 ;
Х к - концентрация растворенного кислорода в пробе анализируемой воды после 5 сут инкубации, мг/ дм 3 ;
Биохимическое потребление кислорода в пробах разбавляющей воды, мг/дм 3 ;
P - степень разбавления пробы, равная 1000/V, где V - объем анализируемой воды в 1 дм 3 смеси после разбавления пробы.
12.4. За результат БПК 5 принимают среднее арифметическое результатов измерения в двух склянках ` X , мг/дм 3 , подвергавшихся инкубации, если расхождение между ними не превышает величины предела повторяемости. В противном случае проводят повторное титрование аликвоты пробы, как описано в . Если и в этом случае расхождение превышает допустимое, результат определения признают недостоверным.
Результат измерения в документах, предусматривающих его использование, представляют в виде:
` Х ± D (Р = 0,95),(6)
где D - границы характеристик погрешности измерения для данной величины БПК 5 , мг/дм 3 (таблица ).
12.5. Допустимо представлять результат в виде:
` X ± D л (Р = 0,95) при условии D л < D ,(7)
где ± D л - границы характеристик погрешности результатов анализа, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений, мг/дм 3 .
Примечание - Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения D л = 0,84 · D с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности.
12.6. Результаты измерения оформляют протоколом или записью в журнале, по формам, приведенным в Руководстве по качеству лаборатории.
13. Контроль качества результатов измерений при реализации методики в лаборатории
13.1. Общие положения
13.1.1. Контроль качества результатов измерений методики в лаборатории предусматривает:
Контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, погрешности, внутрилабораторной прецизионности).
13.1.2. Периодичность контроля исполнителем процедуры выполнения измерений, а также реализуемые процедуры контроля стабильности результатов выполняемых измерений регламентируются в Руководстве по качеству лаборатории.
13.2. Алгоритм оперативного контроля повторяемости
13.2.1. Оперативный контроль повторяемости осуществляют для каждого из результатов измерений, полученных в соответствии с методикой. Для этого отобранную пробу воды делят на две части, и выполняют измерение в соответствии с разделом .
13.2.2. Результат контрольной процедуры r к , мг/дм 3 , рассчитывают по формуле .
14. Проверка приемлемости результатов, получаемых в условиях воспроизводимости
Расхождение между результатами измерений, полученными в двух лабораториях не должно превышать предела воспроизводимости R . При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение R рассчитывают по формуле
R = 2,77 · s R .(11)
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно раздела 5 ГОСТ Р ИСО 5725-6 или МИ 2881 .
Примечание - Проверка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Федеральная служба по гидрометеорологии и мониторингу
окружающей среды
ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ
«ГИДРОХИМИЧЕСКИЙ ИНСТИТУТ»
СВИДЕТЕЛЬСТВО № 74.24-2005
об
аттестации МВИ
Методика выполнения измерений биохимического потребления кислорода в водах скляночным методом.
разработанная ГУ «Гидрохимический институт» (ГУ ГХИ)
и регламентированная РД 52.24.420-2006
аттестована в соответствии с ГОСТ Р 8.563-96
Аттестация осуществлена по результатам метрологической экспертизы материалов по разработке методики выполнения анализа
В результате аттестации установлено, что методика соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
1. Диапазон измеряемых концентраций, значения показателей точности и ее составляющих при доверительной вероятности Р = 0,95
Значения характеристик погрешности и ее составляющих (Р = 0,95)
2. Диапазон измерений, значения пределов повторяемости и воспроизводимости при доверительной вероятности Р = 0,95
3. При реализации методики в лаборатории обеспечивают:
Контроль исполнителем процедуры выполнения измерений (на основе оценки повторяемости при реализации отдельно взятой контрольной процедуры);
Контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности).
Алгоритм контроля исполнителем процедуры выполнения измерений приведен в РД 52.24.420-2006.
Периодичность контроля исполнителем процедуры выполнения измерений, а также реализуемые процедуры контроля стабильности результатов выполняемых измерений регламентируются в Руководстве по качеству лаборатории.
Значение БПК используется для количественной характеристики присутствующих в воде биохимически разрушающихся загрязнений, разложение которых сопровождается изменением кис-. , лородного баланса водоемов. БПК.5 составляет согласно Терио для бытовых сточных вод около 70%. . от соответствующего значения ХПК, показывающего количество, кислорода, нужное для полного окисления всех органических за-. : грязнений.[ ...]
Учитывая длительность выполнения анализов по БПК (5, 10, 20 суток), для оперативного контроля и управления режимом биохимической очистки вод рекомендуется в каждом отдельном случае в условиях установившегося режима поступления и состава вод иметь график, функционально устанавливающий взаимосвязь между ХПК и БПК. Время выполнения анализа по ХПК (экспресс-методика) около 20 мин. Это позволит вовремя вносить коррективы в технологический режим и сохранить жизнеспособность биоценозов. Способность сточных вод к биохимической очистке характеризуется биохимическим показателем, т.е. отношением БПКп /ХПК.[ ...]
Количество органических веществ, выраженное в величинах БПК.5 в различных дисперсных фракциях городской сточной жидкости, показано в табл. 11.[ ...]
Если на высоконагружаемый фильтр сточная жидкость подается с БПК 5 нач, а уходит после прохождения фильтра и вторичного отстойника с БПК5кои, при суточном слое нагрузки на биофильтр Л м (это все равно, что м;3/м2 сутки), то Мй,(-=БПК5нач Л, а М Мвн-ЪПК5конХ ХЛ = Л(БПК5ка„-БПК5кок).[ ...]
Для очистки сточных вод, содержащих органические соединения с БПК = 5-ч-Ю г/л, применяется анаэробный биохимический процесс в метантенках. Процесс наиболее полно протекает при 45-55°С без доступа воздуха (термофильное сбраживание). Часто метантенки используют для обработки осадков из первичных и вторичных отстойников, после чего осадки легко фильтруются, отделяются и обезвреживаются. В результате распада органических соединений образуются метан, углекислый газ, водород, азот, сероводород, которые сжигают с использованием теплоты отходящих газов для обогрева метантенков.[ ...]
Количество взвешенных веществ, поступающих на фильтры, обычно составляет 10-12,5 мг/л при БПК 5,8-6,8 мг/л. Фильтрат содержит 1,3-2,9 мг/л взвешенных веществ, БПК при этом снижается до 2 мг/л. Таким образом, содержание взвешенных веществ при фильтровании снижается на 70-90%, а БПК на 65-75%.[ ...]
Подробного рассмотрения требует биохимическая потребность сточных вод в кислороде БПК.5. Это объясняется не только тем; что БПК5 сточных вод является одним из показателей, который непосредственно используется для расчетов по спуску сточных вод в водоемы, но и трудностью правильного определения этого показателя. Определение БПКб сточной жидкости сопряжено с большими ошибками, которые чаще всего объясняются специфичностью производственных сточных вод, содержащих наряду с органическими веществами, легко окисляющимися биохимически (т. е. при участии микрофлоры воды), также бактерицидные вещества, которые в малых концентрациях могут тормозить процесс биохимического окисления органических веществ сточных вод. Так, органические ¡кислоты (муравьиная, уксусная, молочная и др.), гликоли, ацетон, метанол и др. окисляются в воде, повышая величину биохимического потребления кислорода БПК5, а соединения меди, никеля, кадмия, цинка, кобальта и другие ингредиенты производственных сточных вод уже в малых концентрациях способны тормозить биохимическое потребление кислорода.[ ...]
Рассмотрим пример, помещенный на яомопрамме в виде пунктирных линий. При пятисуточной БПК- 5 = 56,24 мг/л и константе скорости ¡потребления кислорода /0=0,04 ¡полная БПК будет равна 153 мг/л.[ ...]
Иногда для количественной оценки органических веществ подземных вод используется метод БПК-5 (биохимического потребления кислорода после 5-суточного хранения пробы воды). При этом окисление органических веществ происходит под действием микроорганизмов. Значения ХПК и БПК-5 могут быть близкими в случае, если в воде присутствуют биохимически легко окисляющиеся органические вещества (при этом ХПК = = 1,4 БПК).[ ...]
Содержание органических веществ в воде и сточных водах можно определить косвенным методом по показателям БПК.5, БПКполн, а также ХПК. Значения этих показателей учитываются при расчете нагрузки на сооружения биологической очистки сточных вод, выборе конструкции биоокислителей и проверке правильности анализа сточных вод . По разнице между ХПК и БПКполн определяют в сточных водах и воде содержание трудноокисляемых органических веществ и рассчитывают необходимую конструкцию сооружений с более интенсивной биологической очисткой. Описан метод непрерывного автоматического определения органических веществ в воде и сточных водах; одновременно определялись также БПКэ и ХПК сточных вод .[ ...]
Расплывающиеся на воздухе кристаллы с запахом аммиака; М 105,14; т. пл. 28 °С; т. кип. 268 °С; хорошо растворим в воде; БПК.5 0,1; ХПК 1,06.[ ...]
В состав очистных сооружгний поселка Лоза Загорского района входят два высоконагружаемых биофильтра диаметром 15 м, высотой 3,5 м, загруженных щебнем крупностью 40-60 мм. Сточная вода распределяется в биофильтре с помощью реактивного оросителя. Воздух подается двумя вентиляторами ЭВР-4. Гидравлическая нагрузка составляет около 10 м3/(м2-сутки), количество подаваемого воздуха - 12 м3 на 1 м3 воды. На очистные сооружения поступают производственные сточные воды в количестве 1000 м3/сутки и бытовые сточные воды жилого поселка в количестве 500 м3/сутки. БПК.5 поступающих сточных вод составляет примерно 80-130 мг/л, а БПК5 очищенных сточных вод - 4- 16 мг/л.[ ...]
Работа преаэраторов оценивается в комплексе с первичными отстойниками по степени задержания взвешенных веществ и снижению БПК.5. Эффект работы преаэраторов зависит от концентрации сточной воды, количества подаваемого активного ила и конструкции первичного отстойника. Эффект от преаэрации повышается с увеличением концентрации сточных вод.[ ...]
Сточные воды заводов безалкогольных напитков характеризуются нейтральной активной реакцией (pH =7), они содержат 200 мг/л взвешенных веществ; БПК.5 этих стоков составляет 400 мг/л.[ ...]
По оси абсцисс отложены пятисуточные БПК (5). лежащие в пределах 1-1200 мг/л. По линии ординат отложены пол ные БПКо от 2,5 до 2000 мг/л. Прямыми, имеющими подъема слева направо, ¡показаны константы скорости ¡потребления кисло рода в пределах от 0,01 до 0,4.[ ...]
Пусть известно, что промежуток времени между протеканием воды от пункта А до ¡пункта Б равен ¿=14,1 суток, константа скорости (потребления кислорода К1 =0,04 и начальная БПК в точке А равна 5,0 мг/л. Восстанавливаем в точке ¿=14,1 перпендикуляр до встречи с кривой, для которой АТ, =0,04. Из точки пересечения этих двух линий ¡проводим горизонталь до встречи с наклонной, для которой БПК=5,0 мг/л. Из точки пересечения этих двух линий опускаем перпендикуляр на верхнюю горизонталь, которая даст БПК=1,33 мгЦл.[ ...]
Перегрузка первичных отстойников и сокращение времени отстаивания до 1 ч приводит к тому, что в отстойнике задерживается всего 25-30% взвешенных веществ и около 10-15% БПК.5. Следовательно, основная доля по.переработке загрязнений падает на аэротенки, нагрузка ¡на активный ил увеличивается до 460- 500 мг/г ила. Такой активный ил обычно вспухает, особенно в летний период, иловой индекс повышается до 200-300 мл/г. В условиях повышения илового индекса приходится снижать дозу ила в аэротенках, так как не справляются с работой вторичные отстойники, снижение дозы ила увеличивает и без того высокую нагрузку на ил. Приходится увеличивать расход воздуха (до 80- 100 м3 на кг БПКб). Одновременно увеличивается прирост активного ила (он достигает 15-20 т на 100 тыс. м3 сточных вод), что приводит к нарушению работы илоуплотнителей и всей цепочки сооружений по обработке осадка.[ ...]
Кроме основных элементов состава клетки (С, N. О, Н) для ее построения необходимы в незначительном количестве и другие компоненты. Так, потребность клетки в марганце составляет 10-10-5 мг на 1 мг снятой БПК.5, меди- 14,6 -10-5, цинке- 16-10-5, молибдене - 43-10 5, селене - 14-10 10, магнии - 30-Ю-4, кобальте - 13-10 5, кальции 62-10-4, натрии - 5-10-5, калии - 45-10- , железе -12-10-3, карбонат-ионе - 27-. 10-4. Содержание указанных элементов в природных водах, из которых затем образуются сточные, обычно достаточно, чтобы полностью удовлетворить требованиям бактериального метаболизма. Часто не хватает азота и фосфора и их добавляют искусственно в виде суперфосфата, ортофосфорной кислоты, аммофоса, сульфата, нитрата или хлорида аммония, мочевины и т. п.[ ...]
Мей (May, 1954) в статье «Очистка сточных вод нефтеперерабатывающих заводов на опытных биофильтрах» пишет, что очистке подвергались сточные воды, содержащие 42-8Ш мг/л нефтепродуктов с БПК 50-650 мг/л при отсутствии сульфидов. Установка включала коагуляторы, первичные отстойники, биофильтры, вторичные отстойники. В качестве коагулянта использовался сернокислый алюминий (35-40 мг/л) и активированная Si02 (5-6 мг/л). В результате коагуляции БПК снижалось на 33%, содержание нефтепродуктов -■ на 9-86%. Нагрузка на биофильтры по БПК.5 менялась от 148 до 444 г в сутки на 1 м3 загрузки биофильтров. В результате фильтрования БПК5 снижалось до 15- 20 мг/л. После биофильтров рекомендуется сточные воды накоплять в прудах в течение 60 суток, а перед выпуском в водоем пропускать их через микропроцеживатели.[ ...]
Подсчитать, как изменится нагрузка Н на ил, если изменить процент регенерации с 25 на 50% при продолжительности аэрации £ = 6,8 ч, дозе ила в собственно аэротенке ал= 1,4 г/л, в регенераторе яр = 5,6 г/л, зольности ила 3.1 = 28%- БПК.5 воды, поступающей в аэротенк, равна 120 мг/л.[ ...]
Реагенты (сернокислый алюминий и известь) дозируются в сточную воду перед аэрируемыми песколовками в количестве, обеспечивающем снижение концентрации фосфора при отстаивании до 1-2 мг/л. Одновременно в процессе отстаивания снижается БПК.5 на 60-65 % и концентрация взвешенных веществ на 80-90 %. При такой высокой степени извлечения загрязнений на стадии механической очистки продолжительность аэрации может быть значительно сокращена.[ ...]
Опыты по очистке сточных вод предприятий вискозного штапеля хлорированным сернокислым железом производил Моттл . Результаты опытов показали, что по сравнению с обычным отстаиванием пр.и использовании этого способа очистки окисляемость снижается на 31,7%, а БПК.5 - на 39,9%. Оптимальная доза реагента- 100-400 мг/л pH - 6,65-11,8; продолжительность отстаивания - 2 часа.[ ...]
Существенным источником жировых отходов служат мясокомбинаты. Их сточные воды по степени загрязнения в 2-10 раз превышают коммунальные и содержат большое количество белков, жиров, протеинов, спиртов, жирных кислот, что предопределяет значительные величины ХПК и БПК. Так, например, Московский мясокомбинат имеет стоки следующего состава, мг/л: жиры до 2300, белки до 2000, взвешенные вещества до 3000, БПК.5 до 1500, ХПК до 8800 (по кислороду).[ ...]
В настоящее время за рубежом находят все более широкое распространение предельно допустимые концентрации вредных химических веществ в воде водоемов и другие стандарты качества воды. В Англии установлены следующие контрольные показатели для качества воды источников бытового водопользования: БПК.5 меньше 4 мг/л, ХПК менее 25 мг/л. Для источников рыбохозяйственного значения эти показатели выше: БПКб от 10 до 4 мг/л, ХПК от 40 до 25 мг/л. В Англии установлены так называемые рабочие нормативы для сточных вод на основе расчетов, обеспечивающих требуемое качество воды в водоеме (1951).[ ...]
Дефицчт воды во многих районах стимулирует применение очищенных городских сточных вод для водоснабжения промышленных предприятий. Для доведения качества очищенных сточных вод до нормы, требуемой при использовании их в промышленном водоснабжении, необходимо производить их доочистку на фильтрах и обеззараживание. Рекомендуется применение скорых песчаных фильтров, позволяющих снизить содержание взвешенных веществ и БПК.5 до 5 мг/л, а также хлорирование (дозы хлора 5-10 мг/л). Доочищенные сточные воды не должны вызывать повышенного биологического обрастания . Опыт использования очищенных городских сточных вод для водоснабжения промышленных предприятий подтверждает перспективность этогб мероприятия.[ ...]
Качество применяемых коагулянтов, т. е. содержание активных веществ в хлорном железе и гашеной извести, определяют не реже раза в неделю и в каждой новой порции перед ее использованием. Степень коагуляции осадка проверяют не реже раза в неделю, обязательно при использовании новой партии коагулянтов и при пуске сооружений в работу после остановки. Не реже раза в декаду анализируют фильтрат (пробы среднесуточные), определяют pH, взвешенные вещества, БПК.5 и плотный остаток.[ ...]
На кафедре канализации МИИГС (С. В. Яковлевым) вместе с сотрудниками Щукинской очистной станции (П. И. Галаниным и А. Н. Дубовой) исследовалась работа биокоагулятора, в который подавалась’биопленка из вторичных отстойников после биофильтров.[ ...]
В водохранилищах водораздельного бьефа, вследствие отстойного эффекта, в среднем на 10% снижается цветность вода; большинство же показателей качества воды сохраняется на том же уровне, что и в Иваньковском водохранилище. Ниже плотины, на участке длиной 80 км, канал не принимает сточных вод. Водотоки, пересекающие трассу канала, пропущены под ним дюкерами или отведены в другие бассейны. Далее на участке длиной 20 км расположены водохранилища водораздельного бьефа - Икшинское и Песшвское, которые имеют небольшие водосборы и пренебрежимо малые источники загрязнений. Качество воды в этих водохранилищах определяется качеством исходной воды Иваньковского водохранилища и внутриводными процессами. Пяловское и Клязьминское водохранилища имеют относительно большие водосборы и получают большие объемы загрязнений. Особое место занимает Учинское водохранилище, имеющее наименьшую водосборную площадь и наибольший объем при большой глубине. По данным Союзгипроводхоза вода по каналу до Пестова (90 км) проходит в течение 4 сут, по Пестовскому и Икшинскому водохранилищам 10 сут. Коэффициенты самоочищения при температуре воды 19°С характеризуются так: БПК-5 - 0,0072; нефтепродукты - 0,0044; цветность - 0,014.
Если анализ проведен правильно, то в координатах БПК – дни эксперимента должна получиться кривая похожая по форме на кривую А.Если же данная кривая не наблюдается, то причиной этого может явиться один или несколько следующих факторов: разгерметизация колбы, задержка развития бактерий, нитрификация, неправильный выбор диапазона измерения. Разгерметизация колбы может привести к тому, что будет наблюдаться кривая Б, или же к отсутствию отклика. В этом случае следует проверить целостность оборудования и правильность установки измерительной головки.
При анализе образцов с недостаточным начальным количеством аэробных бактерий наблюдается кривая типа В. К данному явлению приводит и акклиматизация бактерий. Именно поэтому следует использовать флору, адаптировавшуюся к данному образцу воды.
Выход за измеряемый диапазон может привести к получению графика, схожего с кривой Г. Используйте разбавление образца чтобы устранить данное явление.
Очень важно выбрать диапазон определения БПК так, чтобы значение, высвечиваемое на шкале прибора, лежало в интервале 20 – 40. Если это значение будет меньше 20, то нельзя утверждать, что полученный результат отражает значение БПК с достаточной точностью. Единственным исключением из этого правила является минимальный диапазон определения БПК (1 – 40), в котором точность измерения максимальна.
Если диапазон БПК неизвестен, то для его оценки используйте результаты определения ХПК (химического потребления кислорода) или данные серии анализов БПК с различными объемами или разбавления образца. Второй вариант предпочтительнее, т.к. соотношение БПК/ХПК строго не регламентировано: в России оно принимается примерно равным 0,5; за рубежом – примерно 0,8. Однако, эта процедура понадобится скорее всего лишь однажды, когда будет проводиться первый анализ.
Примером проявления нитрификации (появлением NO2–ионов вследствие окисления ионов аммония) является кривая Ан. Биологическое окисление органического азота в хозяйственных стоках, как правило, наблюдается спустя пять-шесть дней, что связано с более медленным ростом нитрификационных бактерий. Однако аномально высокое значение поглощения кислорода (особенно при анализе выходных вод) объясняется значительным вкладом жизнедеятельности нитрификационных бактерий в общее значение БПК. Для устранения влияния нитрификации используйте ингибитор нитрификации – N-аллилтиомочевину.
Проведение анализа в образцах воды, значение рН в которых отличается от нейтрального, приводит к сильно заниженным результатам. Нейтрализуйте образец при помощи слабого раствора гидроксида натрия или серной кислоты.
Анализируют первоначальную или соответственно разбавленную пробу по разности между содержанием кислорода до и после инкубации при температуре 20 °С, без доступа воздуха и света.
При анализе производственных сточных вод определяют « полное » БПК; процесс ведут до появления азота нитритов в количестве, не превышающем 0,1 мг / л. Потребление кислорода за 5 суток дает очень большие колебания и не характеризует полной потребности сточной воды в кислороде.
Для получения сравнимых результатов следует строго соблюдать условия, при которых во время определения количество присутствующего кислорода соответствовало бы его потреблению. Это соответствие зависи т о т степени разбавления проб с большим БПК, о т применения одной и той же разбавляющей воды и одного и того же способа обработки воды перед анализом. В ряде случаев полезно вычерчивать кривую, отражающую ход изменения БПК во времени.
Предварительная обработка сточной воды.
Определяемая величина БПК зависит от процессов, которые протекают в сточной воде в период между отбором пробы и ее обработкой. Поэтому взятую пробу необходимо обработать тотчас же. Если невозможно выполнить анализ в день отбора пробы, ее сохраняют при низкой температуре в холодильнике, чтобы биохимические процессы, протекающие в пробе, шли с минимальной скоростью. Всю предварительную подготовку пробы (см. определение растворенного кислорода) проводят на месте отбора пробы.
Сточные воды, имеющие после разбавления рН выше или ниже 6-8, должны быть предварительно нейтрализованы. Кислые воды нейтрализуют 1 н. раствором едкого натра, а щелочные - 1 н. раствором серной кислоты или соляной кислоты. Требуемое количество их определяют титрованием отдельной порции сточной воды соответствующим раствором до рН = 7; визуально - по промтимоловому синему, потенциометрически - с применением стеклянного электрода.
Сточные воды, содержащие свободный хлор (очищенная вода, подвергавшаяся обработке хлором или хлорной известью), перед определением БПК должны быть обработаны тиосульфатом натрия.
Объем раствора тиосульфата натрия, необходимого для восстановления свободного хлора, определяют титрованием. К 100 мл пробы прибавляют 10 мл разбавленной серной кислоты (1:50), 10 мл 10 % - ного раствора иодида калия и титруют 0,025 н. раствором тиосульфата н атрия с применением в качестве индикатора раствора крахмала;0,025 н. раствор тиосульфата натрия вследствие его неустойчивости готовят непосредственно перед применением путем разбавления 0,05 н. раствора (см. определение растворенного кислорода). К пробе, предназначенной для определения БПК, прибавляют эквивалентное количество 0,025 н. раствора тиосульфата натрия, рассчитанное по результату титрования. Мешают определению вещества, реагирующие с растворенным кислородом. Влияние таких веществ устраняют увеличением времени между разбавлением пробы водой (или аэрацией) и определением кислорода в кислородной склянке, предназначенной для определения кислорода в день отбора пробы. Определение начинают через час после разбавления пробы.
Аппаратура.
1. Кислородные склянки, калиброванные с точностью до 0,1 мл, вместимостью 100-300 мл.
2. Термостат, установленный на 20 °С, с допустимым отклонением ± 1 °С. Целесообразно применять термостат с водяным охлаждением, который обеспечивает указанную температуру и в летнее время. В термостат помещают мелкие фотографические кюветы, которые после наполнения их дистиллированной водой служат водяными затворами для кислородных склянок. Склянки погружают в них пробками вниз. Воду в кюветах обновляют при каждом определении.
3. Мешалки.
Реактивы.
1. Реактивы те же, что и при определении растворенного кислорода.
2. Дистиллированная вода. Ее получают перегонкой в стеклянном перегонном аппарате. Дистиллированная вода не должна содержать меди и свинца более 0,01 мг / л, цинка более 1 мг / л, едких щелочей, активного хлора и других бактерицидных веществ. Дистиллированная вода выдерживается в бутылях, закрытых марлей, в течение нескольких дней при комнатной температуре.
3. Фосфатный буферный раствор рН = 7,2 . Растворяют 8,5 г KH 2 PO 4 , 21,75 г К 2 НРО 4 , 33,4 г Na 2 HP O 4 × 7 Н 2 O , 1,7 г NH 4 Cl в дистиллированной воде и доводят объем до 1 л (реактивы ч. д. а.).
4 . Сульфат магния. Растворяют 22,5 г М g S 0 4 × 7 H 2 O ч. д. а. в дистиллированной воде и доводят объем до 1 л.
5 . Хлорид кальция. В дистиллированной воде растворяют 2,5 г CaCl 2 безводного, ч. д. а. и доводят до 1 л.
6 . Хлорид железа (III). Растворяют 0,25 г F eCl 3 × 6Н 2 О ч. д. а. в дистиллированной воде и доводя т до 1 л.
7 . Разбавляющая вода. Прибавляют к 1 л дистиллированной воды по 1 мл фосфатного буферного раствора, растворов сульфата магния, хлорида кальция и хлорида железа (III) . После прибавления солей воду хорошо перемешивают. Разбавляющую воду приготавливают в день ее применения. При температуре 20 °С она должна содержать приблизительно 8,8 мг / л растворенного кислорода.
8 . Разбавляющая вода с добавками. Готовится непосредственно перед применением. К 1 л разбавляющей воды прибавляют 1 мл отстоявшейся хозяйственно - бытовой сточной воды (сохранявшейся не более 24 ч) или 10-20 мл речной воды. Взамен этих добавок рекомендуется (особенно при анализе промышленных сточных вод) вводить культуру микроорганизмов, выращенных на анализируемой воде.
Для приготовления культуры микроорганизмов анализируемую сточную воду разбавляют водопроводной водой в 10-100 раз в зависимости от концентрации в ней органических веществ прибавляют 2-3 капли раствора реактивов, применяемых для приготовления разбавляющей воды, и оставляют в открытом сосуде на два - три дня. Появление мути или пленки указывает на развитие микрофлоры (проверяют под микроскопом). Микрофлору переносят в пробу анализируемой сточной воды, разбавленную в 5-20 раз; после дальнейшего развития флоры отбирают 1 мл этой жидкости.
При определении БПК в биологически очищенных сточных водах внесение указанных добавок в разбавляющую воду не требуется.
Примечание. Результаты определения БПК в пробах, разбавленных водой с добавками, должны быть скорректированы по количеству кислорода, поглощенного прибавленными веществами. Для этого определяют обычным способом БПК хозяйственно - бытовой сточной вода или речной воды, применявшихся в качестве добавок. По величине БПК определяет поправку, представляющую собой расход кислорода на то количество добавки, которое находится в 1 л смеси анализируемой пробы с разбавляющей водой. Поправку вычитают из величины определенного БПК исследуемой смеси.
Разбавление сточной воды.
Необходимое разбавление сточной воды ориентировочно рассчитывают по результатам определения бихроматной окисляемости (ХПК). Условно принимают, что БПК составляет 50 % от ХПК, а так как в воде после инкубации при правильно взятом разбавлении должно оставаться примерно 4-5 мг О 2 / л, то вычисленное значение БПК делят на 4 или 5. Полученный результат показывает, во сколько раз надо разбавлять анализируемую воду.
Пример. Бихроматная окисляемость сточной воды 500 мг О 2 / л. Принимаем БПК равным 50 % от ХПК, т. е. 250 мг / л. Делим эту величину на 5, получаем, что сточную воду надо разбавить в 50 раз. Можно делать два разбавления, принимая условно БПК за 60 и 40 % от величины ХПК.
При разбавлении необходимо следить за тем, чтобы разбавляющая вода и полученная в результате разбавления смесь имели температуру 18-20 °С, а рН смеси не выше 8 и не ниже 7.
Правильность разбавления контролируют следующим образом. После всего периода инкубации концентрация кислорода в сточной воде должна быть не менее 3 мг / л и потребление кислорода за весь период инкубации - также не менее 3 мг / л.
Для сточной воды, прошедшей биоокислители, этот способ расчета разбавления неприменим, так как в очищенной жидкости могут оставаться вещества, не поддающиеся дальнейшему распаду под влиянием микроорганизмов, но окисляющиеся бихроматным методом, т. е. дающие высокую ХПК. В этом случае разбавление осуществляют, исходя из наличия нитратов в очищенной воде. Обычно при концентрации нитратов 5- 10 мг / л БПК полное будет не выше 15-20 мг / л. Следовательно, очищенную воду нужно разбавить максимально в 5 раз. Лучше разбавлять дважды - в 2 и 5 раз.
В мерную колбу необходимой вместимости наливают посредством сифона (чтобы в колбу не попали пузырьки воздуха) разбавляющую воду до половины колбы, прибавляют точно отмеренное пипеткой количество исследуемой воды и доливают до метки разбавляющую воду. Закрыв колбу пробкой, тщательно перемешивают содержимое, перевертывая колбу 15-16 раз.
Ход определения.
Разбавленную сточную воду разливают с помощью сифона в кислородные склянки для инкубации, наполняя их доверху, и закрывают косо срезанными притертыми пробками так, чтобы не оставалось пузырьков воздуха. Затем эту же воду наливают в колпачки от склянок и, перевернув склянки вверх дном, вставляют их в колпачки, вытесняя из последних воду так, чтобы пузырьки воздуха не попали в колпачки. После этого склянки ставят в нормальное положение.
Одновременно наполняют такое же количество склянок разбавляющей водой. Каждой пробе анализируемой сточной воды должна соответствовать одна склянка с разбавляющей водой.
В одной из склянок с испытуемой водой и в одной из склянок с разбавляющей водой сразу же определяют растворенный кислород. Все остальные склянки помещают в термостат при температуре 18-20 °С и держат в нем в течение необходимого времени.
При определении кинетики биохимического потребления кислоро да в зависимости от времени длительность инкубационного периода составляет 2; 5; 10; 15; 20; 25 суток. Исходя из этого устанав ли вают число заполняемых кислородных склянок.
Через указанные промежутки времени от начала инкубации вынимают из термостата по одной склянке с анализируемой и разбавляющей водой и определяют в них растворенный кислород и содержание нитритов. Нитриты определяют в воде, налитой в колпачок склянки, который снимают так же, как надевали, т. е. перевернув склянку вверх дном. Если в пробе начался процесс нитрификации, что обнаруживается по появлению в воде нитритов в концентрации, превышающей 0,1 мг / л, то дальнейшее определение БПК (для более продолжительного времени инкубации) не проводят. Если на пятые сутки появляются следы нитритов, то следующее определение проводят через 7-8 суток.
Содержание нитритов может быть определено колориметрически. Вместо склянок с пришлифованными стеклянными колпачками для контроля процесса нитрификации можно поставить в термостат дополнительно 12 неградуированных склянок любого размера, наполненных той же водой (анализируемой и разбавляющей), и в них определять содержание нитритов после каждого срока инкубации. Склянки помещают в сосуд, наполненный небольшим количеством дистиллированной воды, пробками вниз, так, чтобы горлышко склянок было погружено в воду (водяной затвор). Дистиллированную воду в сосуде обновляют при каждом определении. В этом случае, если в конце периода инкубации содержание нитритов будет больше 0,1 мг / л, растворенный кислород определяют с добавлением азида натрия, сульфаминовой кислоты или мочевины (см. определение растворенного кислорода).
Определение БПК считается более точным в тех пробах, в которых нитрификация только началась.
Биохимическое потребление кислорода за определенный период инкубации вычисляют по формуле:
где a 1 и a 2 - концентрация кислорода в начале инкубации (в « нулевой день »), соответственно в подготовленной для определения пробе и в разбавляющей воде, в мг / л;
в 1 и в 2 - концентрация кислорода в конце инкубации соответственно в пробе и в разбавляющей воде, в мг / л;
У - объем сточной воды, содержащейся в 1 л пробы после всех проведенных разбавлений, в мл.
Похожая информация.